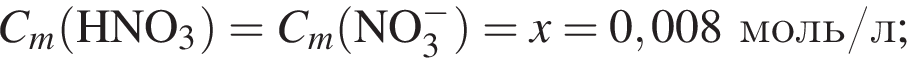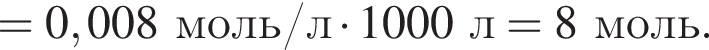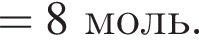Одноатомными молекулами (н. у.) образовано простое вещество:
Укажите символ химического элемента:
Основные свойства высших оксидов предложенных элементов монотонно усиливаются в ряду:
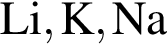
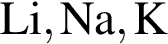
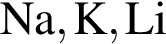
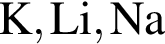
Ионные связи содержатся во всех веществах ряда:
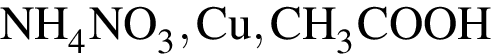
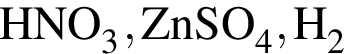
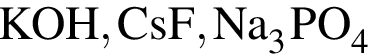
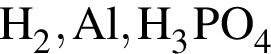
В порядке увеличения температур кипения вещества расположены в ряду:
Веществом, образующим альдегид при взаимодействии с водой 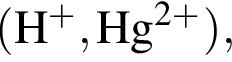 является:
является:
К классу альдегидов относится вещество, название которого:
В атоме химического элемента ![]() в основном состоянии электроны распределены по энергетическим уровням следующим образом: 2, 8, 5. Степень окисления
в основном состоянии электроны распределены по энергетическим уровням следующим образом: 2, 8, 5. Степень окисления ![]() в высшем оксиде равна:
в высшем оксиде равна:
В отличие от разбавленной концентрированная серная кислота:
а) вытесняет ![]() из твёрдого
из твёрдого ![]() ;
;
б) НЕ реагирует с медью;
в) реагирует с  ;
;
г) при взаимодействии с цинком НЕ образует водород.
Для реакции 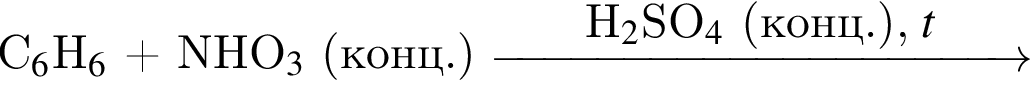 укажите верные утверждения:
укажите верные утверждения:
а — реакция отщепления
б — реакция замещения
в — органический продукт реакции — нитробензол
г — органический продукт реакции содержит серу
Два кислотных оксида образуются в результате химического превращения:
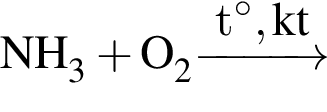 ;
;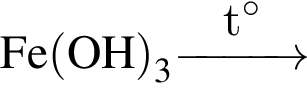 ;
;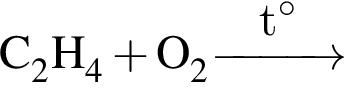 ;
;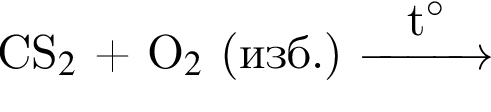 .
.Выберите утверждения, верно характеризующие магний:
а) реагирует с горячей водой с образованием щёлочи;
б) массовая доля в его фосфиде равна 60,8 %;
в) можно получить электролизом расплава его иодида;
г) при его участии осуществляется процесс фотосинтеза.
Выберите утверждения, верно характеризующие этин:
а) в молекуле две ![]() -связи;
-связи;
б) молекула имеет угловое строение;
в) обесцвечивает бромную воду;
г) при 20 °C представляет собой хорошо растворимую в воде жидкость.
На графике представлена зависимость количеств исходного вещества (А) и продукта (В) от времени протекания некоторой реакции. В уравнении этой реакции коэффициент перед формулой А равен 2. Определите коэффициент перед формулой В:
Водный раствор фенолфталеина окрасится, если к нему добавить:
В отличие от метанола пропанол-1 вступает в реакцию:
Установите соответствие между названием органического вещества и общей формулой гомологического ряда, к которому относится данное вещество.
А) 2-метилпропанол-1
Б) бутадиен-1,3
В) метилформиат
Г) ацетилен
1) ![]()
2) 
3) 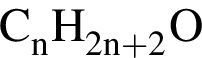
4) 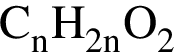
5) 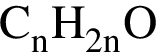
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б2В5Г1.
Определите коэффициент перед формулой продукта восстановления в уравнении химической реакции, протекающей по схеме:
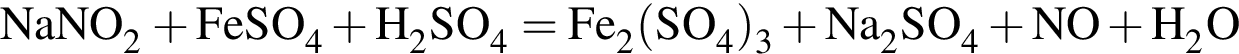
В четырёх пронумерованных пробирках находятся растворы неорганических веществ. О них известно следующее:
— вещества из пробирок 1 и 4 нейтрализуют друг друга;
— вещества из пробирок 3 и 4 реагируют между собой с образованием осадка, который растворяется как в кислотах, так и в щелочах;
— при добавлении к содержимому пробирки 2 вещества из пробирки 4 образуется осадок, который на воздухе приобретает бурую окраску.
Установите соответствие между названием неорганического вещества и номером пробирки, в которой находится раствор данного вещества.
А) сульфат цинка
Б) азотная кислота
В) хлорид железа(II)
Г) гидроксид натрия
1
2
3
4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б4В3Г1.
Будет наблюдаться выпадение белого осадка при добавлении бромной воды к обоим веществам
1) олеиновой кислоте и гексану
2) бензолу и фенолу
3) анилину и фенолу
4) изопрену и бензолу
Расставьте коэффициенты методом электронного баланса в уравнении окислительно-восстановительной реакции, схема которой
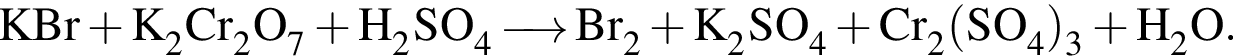
Укажите сумму коэффициентов перед веществами молекулярного строения.
К раствору сульфата меди(II) массой 800 г с массовой долей 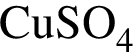 7% добавили медный купорос массой 80 г и персмешали смесь до полного его растворения. Рассчитайте массовую долю (%) соли в полученном растворе.
7% добавили медный купорос массой 80 г и персмешали смесь до полного его растворения. Рассчитайте массовую долю (%) соли в полученном растворе.
Дана схема превращений
Определите сумму молярных масс (г/моль) органических веществ ![]() и
и ![]() .
.
Зеленовато-жёлтый газ А (примерно в два с половиной раза тяжелее воздуха) реагирует с самым лёгким газом Б с образованием вещества В. Водный раствор вещества В является сильной кислотой. При взаимодействии В с газом Г, образующимся при действии гидроксида натрия на соли аммония, образуется соль Д, использующаяся при пайке. Найдите сумму молярных масс (г/моль) веществ В и Д.
При добавлении к раствору кислой соли А соляной кислоты выделяется газ Б. Газ Б не поддерживает горение. При пропускании Б через известковую воду выпадает осадок В, который растворяется в избытке Б. Газ Б образуется при сгорании углеводородов. При добавлении к раствору кислой соли А гидроксида натрия образуется газ Г (легче воздуха), имеющий резкий запах. Газ Г вызывает посинение влажной лакмусовой бумажки. При окислении газа Г в присутствии ![]() образуется несолеобразующий оксид Д. Укажите сумму молярных масс (г/моль) кислой соли А и несолеобразующего оксида Д.
образуется несолеобразующий оксид Д. Укажите сумму молярных масс (г/моль) кислой соли А и несолеобразующего оксида Д.
Определите сумму молярных масс (г/моль) азотсодержащих веществ ![]() и
и ![]() образовавшихся в результате превращений, протекающих по схеме
образовавшихся в результате превращений, протекающих по схеме
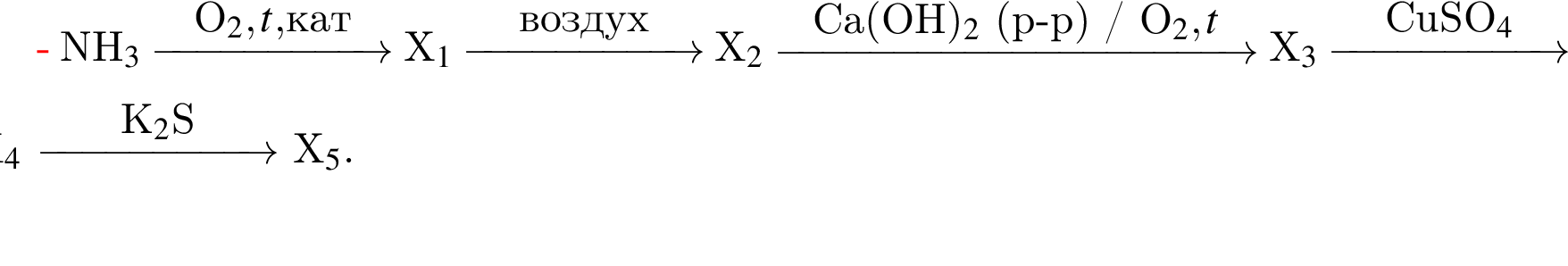
В четырех пронумерованных пробирках находятся растворы неорганических веществ. О них известно следующее:
— вещества из пробирок 2 и 3 нейтрализуют друг друга, способны растворять цинк, его оксид и гидроксид;
— вещества из пробирок 3 и 4 реагируют между собой с образованием осадка, способного растворяться как в кислотах, так и в щелочах;
— при электролизе расплава вещества из пробирки 1 выделяется газ (н. у.) зеленовато-желтого цвета, имеющий характерный запах.
Установите соответствие между содержимым пробирки и ее номером.
А) гидроксид калия
Б) сульфат алюминия
В) азотная кислота
Г) хлорид натрия
1
2
3
4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б1В3Г4.
Выберите четыре утверждения, верно характеризующие аммиак.
| 1 | НЕ реагирует с оксидом кальция |
| 2 | вступает в окислительно-восстановительную реакцию с уксусной кислотой |
| 3 | в водном растворе меняет окраску индикаторов |
| 4 | в промышленности реакция его получения из простых веществ протекает при пониженной температуре |
| 5 | при растворении в воде образует катион аммония и гидроксид-ион |
| 6 | используется для получения аммофоса |
Ответ запишите цифрами (порядок записи цифр не имеет значения), например: 1246.
Установите соответствие между схемой обратимой реакции и направлением смещения равновесия при увеличении давления.
А) 
Б) 
В) 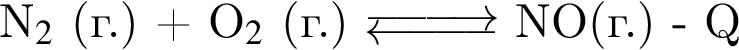
Г) 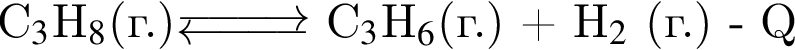
1 — вправо (в сторону продуктов)
2 — влево (в сторону исходных веществ)
3 — НЕ смещается
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А1Б2ВЗГЗ.
Уксусная кислота широко применяется в качестве консерванта (пищевая добавка Е260). В быту чаще всего используют уксус (массовая доля кислоты 9%, 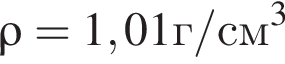 ) или уксусную эссенцию (массовая доля кислоты 70%,
) или уксусную эссенцию (массовая доля кислоты 70%,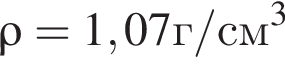 ). Для консервирования овощей требуется 225см3 уксуса. Вычислите, в каком объеме воды (см3) необходимо растворить уксусную эссенцию, чтобы приготовить раствор для консервирования.
). Для консервирования овощей требуется 225см3 уксуса. Вычислите, в каком объеме воды (см3) необходимо растворить уксусную эссенцию, чтобы приготовить раствор для консервирования.
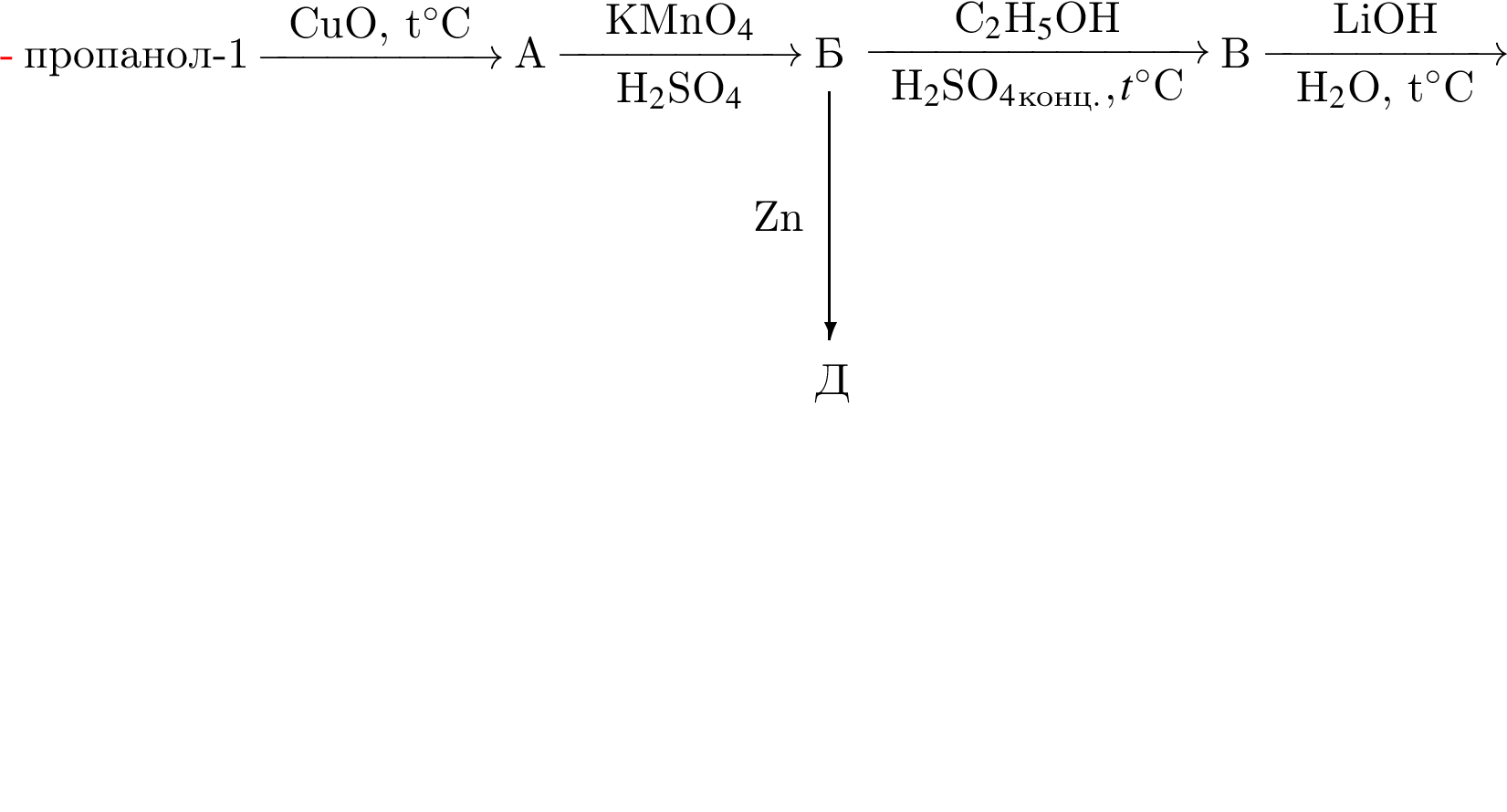
Определите сумму молярных масс (г/моль) органических веществ молекулярного строения А и немолекулярного строения Д и Г, полученных в результате превращений:
Дан перечень неорганических веществ: негашеная известь, оксид фосфора(V), оксид серы(VI), сернистый газ, оксид лития. Определите число веществ, которые могут реагировать с водой при комнатной температуре
В каждый из пяти стаканов, наполненных разбавленными водными растворами, поместили по одной медной монете.
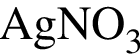
![]()
![]()
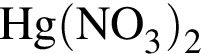
![]()
Определите число стаканов, в которых масса монеты НЕ изменилась.
Для анализов смеси хлоридов натрия и аммония провели следующие операции. Навеску смеси массой 5г растворили в воде. К полученному раствору прибавили 300г раствора гидроксида калия с массовой долей ![]() 2,8% и нагрели до полного удаления аммиака. В образовавшийся раствор добавили метиловый оранжевый, а затем акуратно прибавляли соляную кислоту, пока среда раствора не стала нейтральной. Объем израсходованной кислоты равен 150см3, концентрация HCl в кислоте 0,5моль/дм3. Вычислите массовую долю(%) хлорида аммония в исходной смеси.
2,8% и нагрели до полного удаления аммиака. В образовавшийся раствор добавили метиловый оранжевый, а затем акуратно прибавляли соляную кислоту, пока среда раствора не стала нейтральной. Объем израсходованной кислоты равен 150см3, концентрация HCl в кислоте 0,5моль/дм3. Вычислите массовую долю(%) хлорида аммония в исходной смеси.
Расположите водные растворы веществ в порядке уменьшения их pH:
1) 0,5 моль/дм3 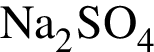
2) 0,5 моль/дм3 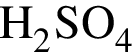
3) 0,5 моль/дм3 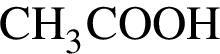
4) 0,5 моль/дм3 ![]()
В избытке воды растворили 25 г медного купороса, а затем — 14 г сульфида бария. Образовавшуюся смесь профильтровали, осадок отделили и высушили. Вычислите массу (г) полученного в результате эксперимента твердого остатка.
Составьте полные ионные уравнения реакций. Установите соответствие между реакцией и суммой коэффициентов в правой части полного ионного уравнения. Все электролиты взяты в виде разбавленных водных растворов.
A) 
Б) 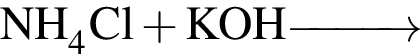
B) 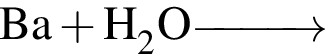
Г) 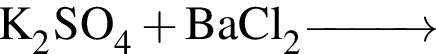
1) 1
2) 2
3) 3
4) 4
5) 5
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А1Б4В3Г5.
В растворе, полученном добавлением азотной кислоты к разбавленной серной кислоте, суммарная молярная концентрация анионов равна 0,009 моль/дм3, а значение pH 2. Считая, что обе кислоты полностью распадаются на ионы, вычислите количество (моль) азотной кислоты в этом растворе объемом 1 м3.

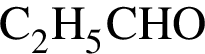 — один из простейших представителей этого класса.
— один из простейших представителей этого класса.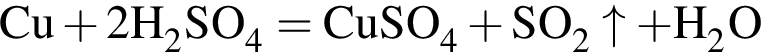 );
);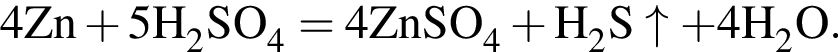
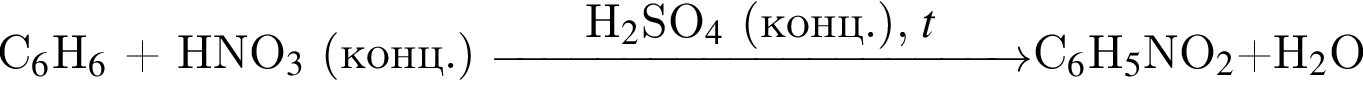
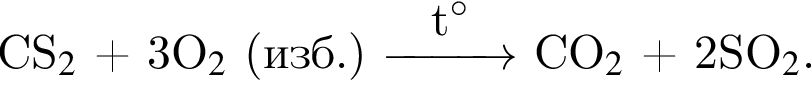
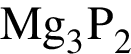 примерно равна 53,73 %;
примерно равна 53,73 %;
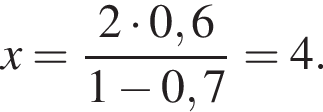
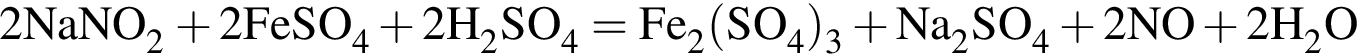
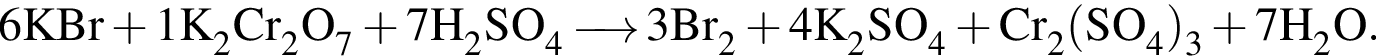
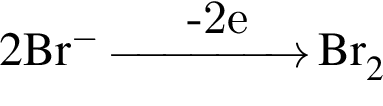
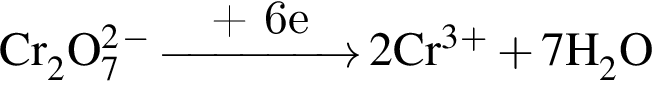
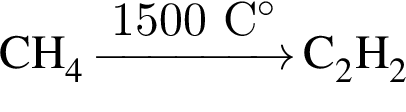
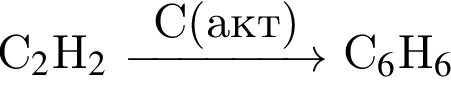
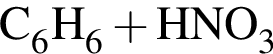 →
→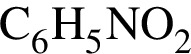
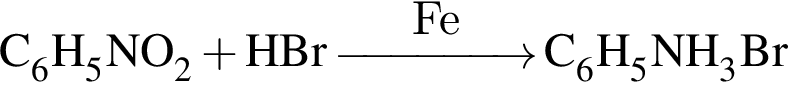
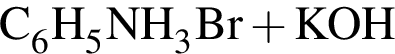 →
→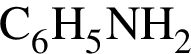
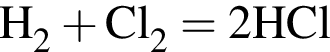 );
);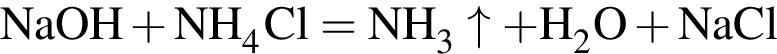 );
);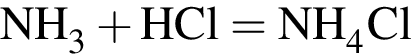 ).
).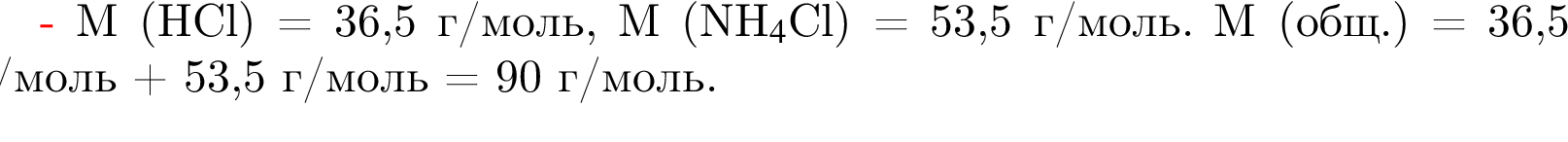
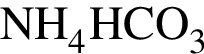 );
);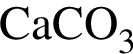 );
);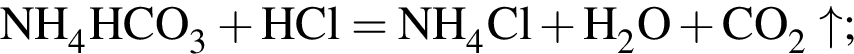
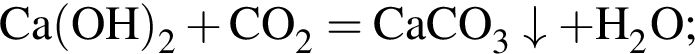
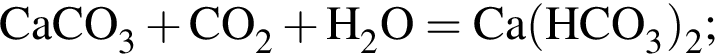
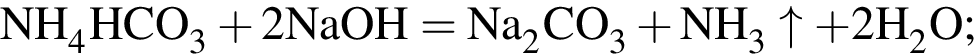
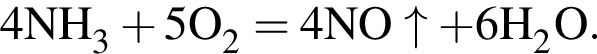
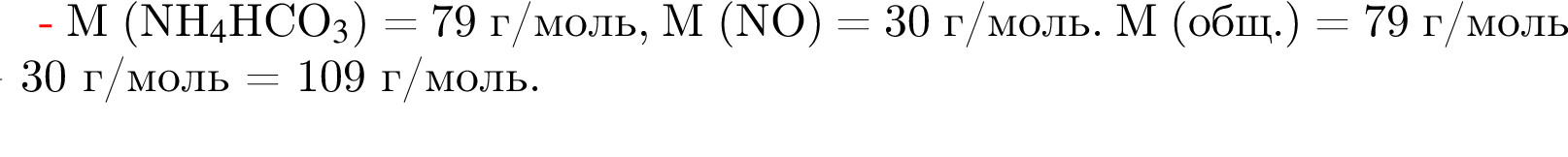
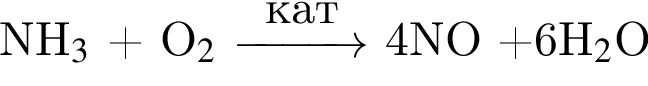
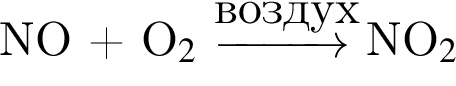
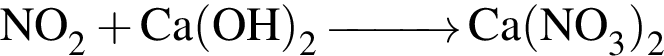

 ↓
↓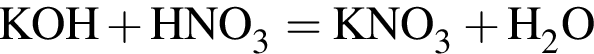
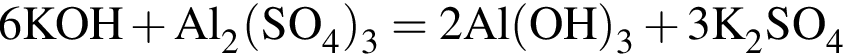
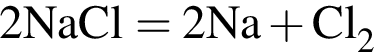 (зеленовато-жёлтый газ)
(зеленовато-жёлтый газ)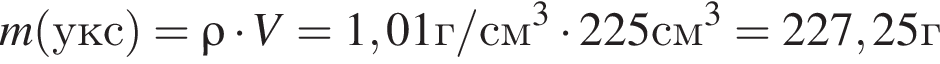


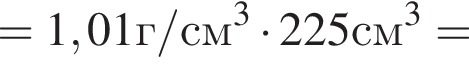

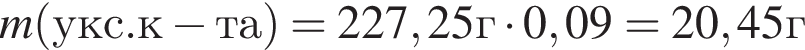
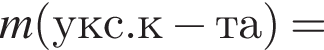
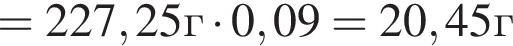
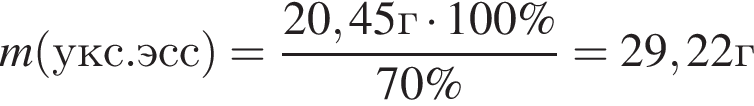
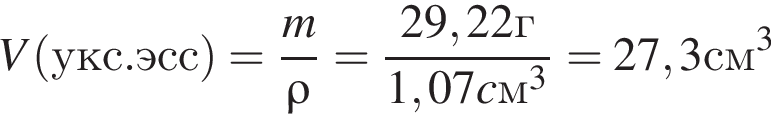
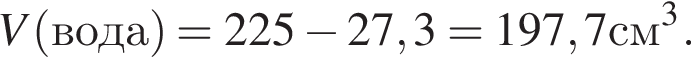 Округлив до целых, получим 198см3.
Округлив до целых, получим 198см3.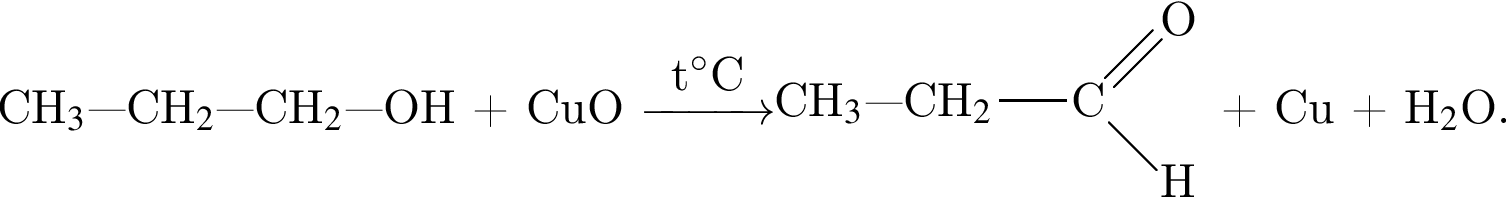


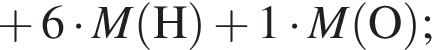

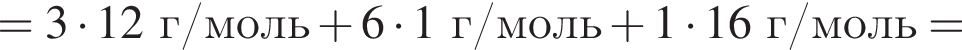
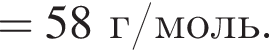
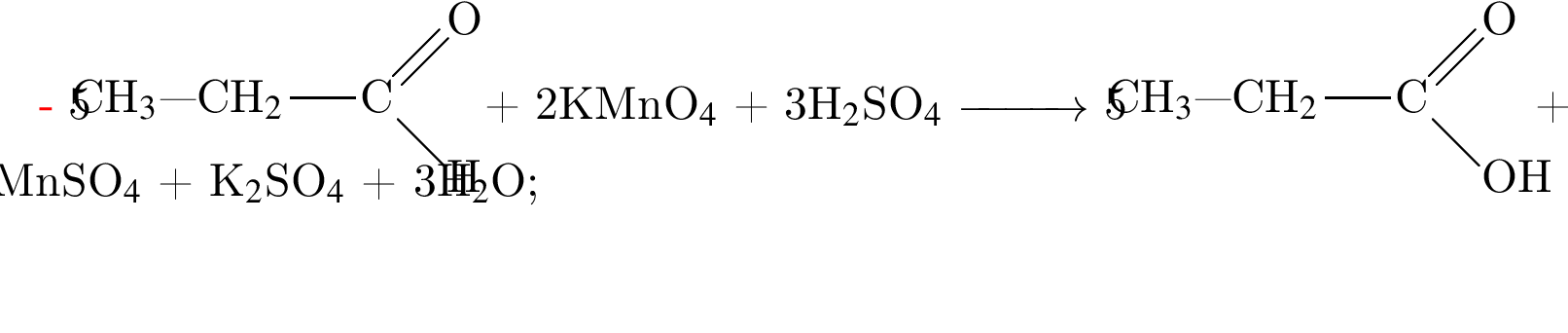
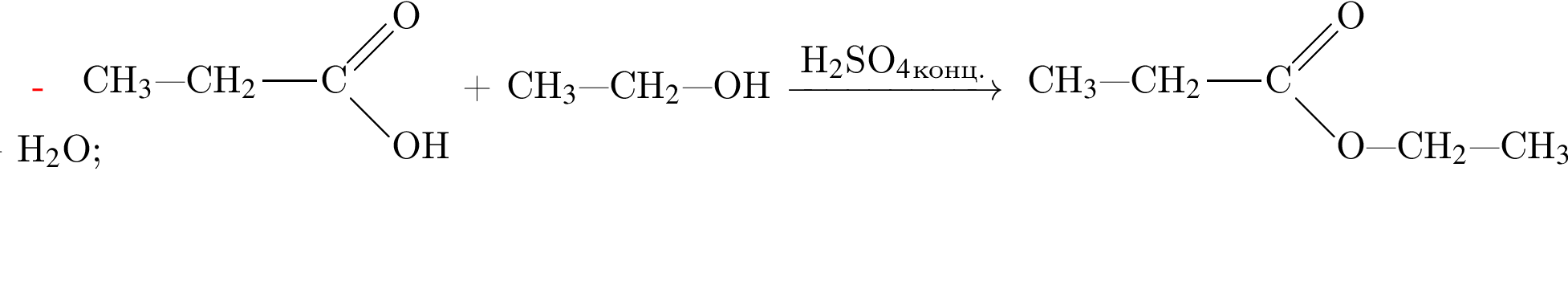
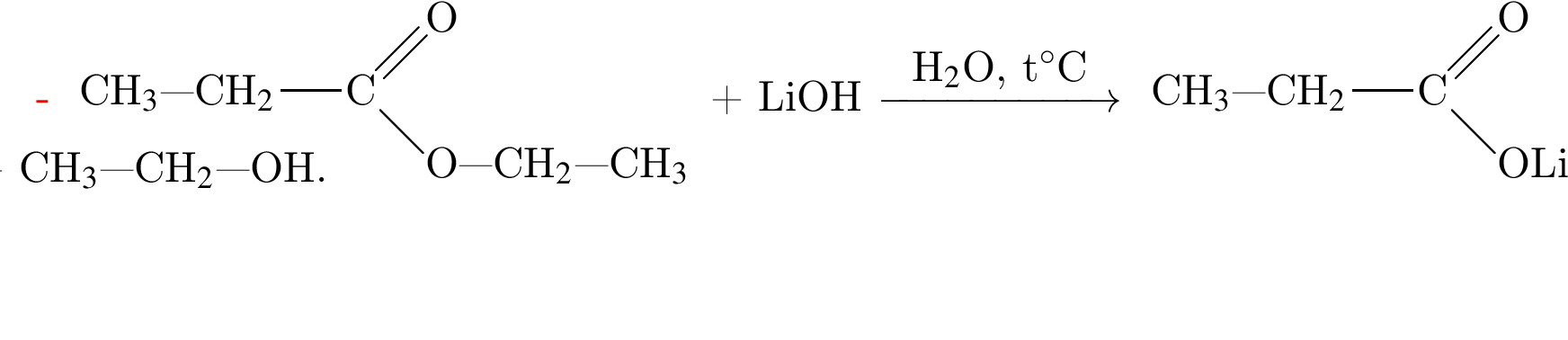
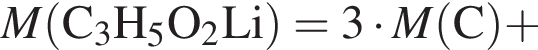
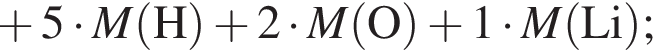
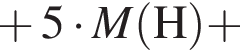
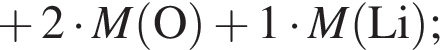
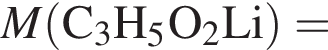

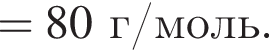
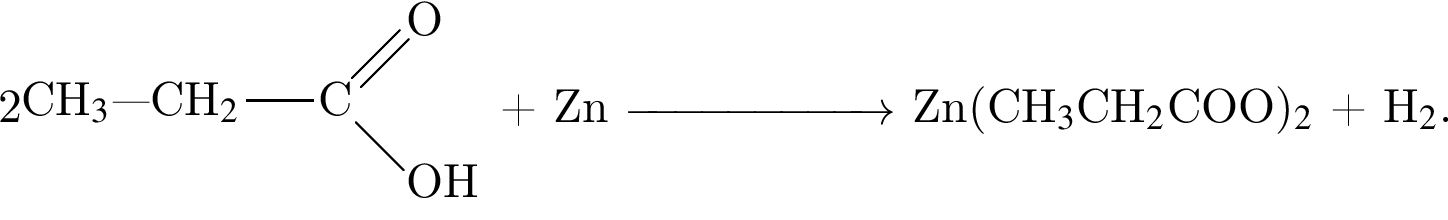

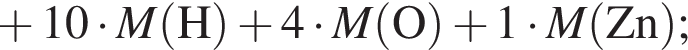
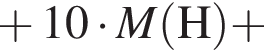



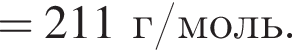
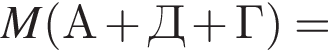
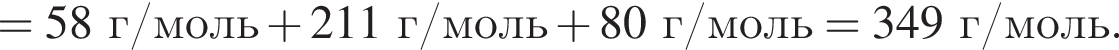
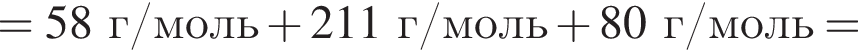
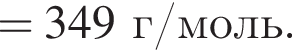
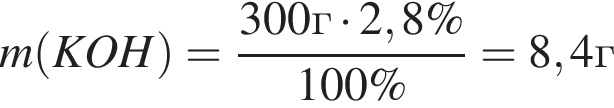
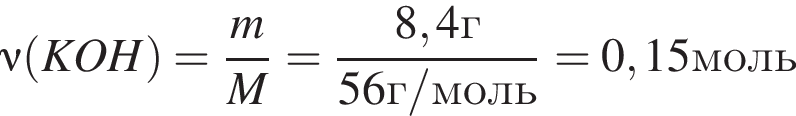
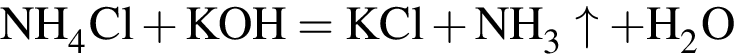 , оставшийся
, оставшийся 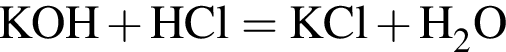
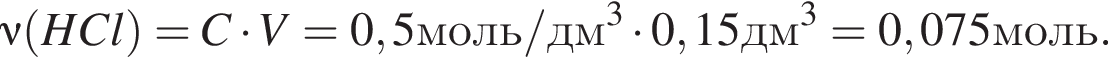

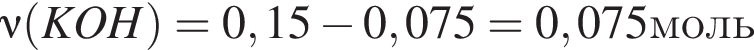 прореагировало с
прореагировало с 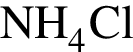 .
. Найдем массу хлорида аммония:
Найдем массу хлорида аммония:

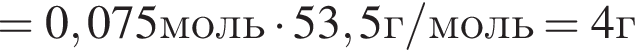
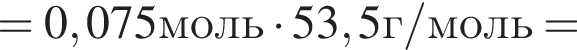
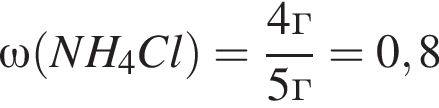 (80%)
(80%)

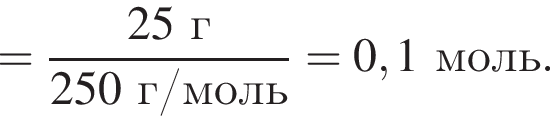

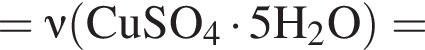

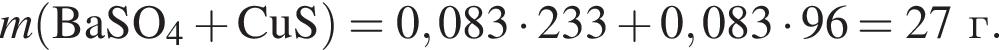
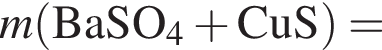
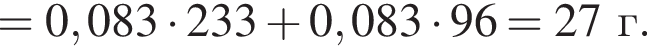
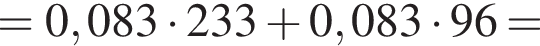

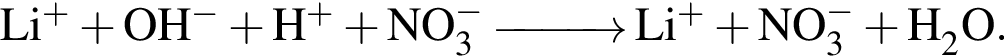 Сумма коэффициентов в правой части — 3.
Сумма коэффициентов в правой части — 3. Сумма коэффициентов в правой части — 4.
Сумма коэффициентов в правой части — 4.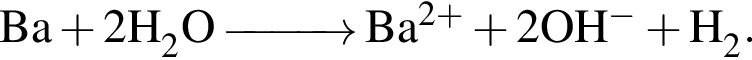 Сумма коэффициентов в правой части — 4.
Сумма коэффициентов в правой части — 4.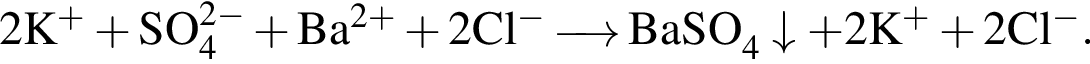 Сумма коэффициентов в правой части — 5.
Сумма коэффициентов в правой части — 5.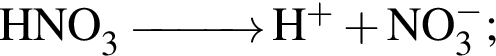
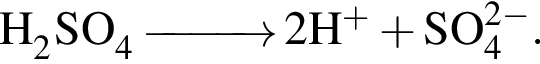

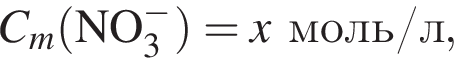 а
а 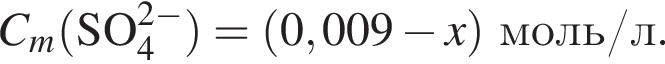 Так как
Так как  то
то 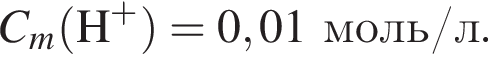 Исходя из условия электронейтральности получим следующее уравнение и решим его:
Исходя из условия электронейтральности получим следующее уравнение и решим его:  откуда
откуда 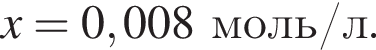 Значит,
Значит,